Projekte Virale Proteomik

Wege hin zu einer personalisierten Prävention und Behandlung von schwerer Norovirus-Gastroenteritis (Paving the Way towards Personalized Prevention and Care of Severe Norovirus Gastroenteritis, PRESENt)
Noroviren verursachen einen Großteil der Gastroenteritiden, wobei individuelle Parameter Anfälligkeit und Verlauf der Infektion beeinflussen. Akute Ausbrüche z.B. auf Kreuzfahrtschiffen oder in Altenpflegeeinrichtungen sowie chronische Infektionen in immungeschwächten Patienten stellen ein erhöhtes Gesundheitsrisiko dar. Dennoch gibt es bisher weder einen Impfstoff noch eine spezifische Therapie zur Vorbeugung oder Behandlung von Norovirus-Infektionen. Auch ist nicht bekannt, was die individuellen Unterschiede in der Anfälligkeit und im Infektionsverlauf ausmacht. Um die Ursachen dieser Varianzen aufzuklären, bündeln die PRESENt Partner vom TWINCORE, der Medizinischen Hochschule Hannover, dem L3S Forschungsinstitut und dem Helmholtz-Zentrum für Infektionsforschung ihre Expertisen am neu in Hannover entstehenden Zentrum für Individualisierte Infektionsmedizin (Centre for Individualised Infection Medicine, CiiM). Mittels datenintensiver Technologien und ‚machine learning‘ Methoden werden die PRESENt Partner aufdecken, welche individuellen Parameter die Norovirus-Infektion beeinflussen. Hierzu werden in einer retrospektiven Studie individuelle Parameter wie Geschlecht, Alter und Vorerkrankungen mit den klinischen Daten in Relation gesetzt und Muster für den Infektionsverlauf berechnet. In einer prospektiven klinischen Studie werden die Forscher zudem das Mikrobiom, die Virusbeschaffenheit im Hinblick auf die Assoziation mit menschlichen Biomolekülen sowie klinische Parameter erheben und Muster berechnen. Gleichzeitig wird das Konsortium die Effektivität von Desinfektionsmitteln für die individuellen Patientenproben in modernen in vitro Modellen (sogenannte Organoide) testen. Basierend auf diesen Erkenntnissen sollen Strategien für eine personalisierte Prognose, Prävention und Behandlung schwerer Norovirus-Infektionen entwickelt werden.
Kooperationspartner: Prof. Dr. Wolfgang Nejdl (Leibniz Universität Hannover & Technische Universität Braunschweig, Forschungszentrum L3S Hannover), Prof. Dr. Dr. Michael Marschollek (Medizinische Hochschule Hannover, Peter L. Reichertz Institut für Medizinische Informatik der TU Braunschweig und der Medizinischen Hochschule Hannover), Prof. Dr. Till Strowig, Prof. Dr. Lothar Jänsch (Helmholtz-Zentrum für Infektionsforschung Braunschweig), PD Dr. Benjamin Heidrich (Medizinische Hochschule Hannover, Klinik für Gastroenterologie, Hepatologie und Endokrinologie Hannover), Prof. asoc. inv. Dr. Gisa Gerold (Medizinische Hochschule Hannover, TWINCORE - Zentrum für experimentelle und klinische Infektionsforschung Hannover)
Koordinatorin des Konsortiums: Prof. asoc. inv. Dr. Gisa Gerold
Kollaborierende Gruppen: Prof. Dr. Thomas F. Schulz (Medizinische Hochschule Hannover, Institut für Virologie), Prof. Dr. Lennart Svensson (Linköping University Schweden)
Gefördert durch das Niedersächsische Ministerium für Wissenschaft und Kultur und die VolkswagenStiftung im Rahmen der Ausschreibung „Big Data in den Lebenswissenschaften der Zukunft“
Charakterisierung von CD81 Rezeptor-Interaktionen bei der Hepatozyten Invasion von Hepatitis C Virus und Plasmodium
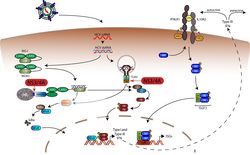
Hepatitis C Virus (HCV) und der Malaria Erreger Plasmodium falciparum nutzen beide das humane Transmembranprotein CD81, um Leberzellen zu infizieren. Dies ist bemerkenswert, da sich beide Pathogene hinsichtlich ihres molekularen Aufbaus, ihrer Übertragung und den von ihnen ausgelösten Krankheiten stark unterscheiden. Eine Gemeinsamkeit ist lediglich der enge Wirtstropismus: Beide Erreger infizieren unter natürlichen Umständen ausschließlich Menschen. CD81 ist einer von mehreren Faktoren, die diesen Wirtstropismus bestimmen. Es wird angenommen, dass CD81 die Aufnahme von HCV und Plasmodium über Protein-Protein Interaktionen mit Membran-nahen Signalmolekülen und Zytoskelettregulatoren initiiert.
In unserer bisherigen Forschung gelang es uns, 33 CD81 Protein Interaktionen in humanen Hepatomzellen zu identifizieren, wobei mindestens zehn der interagierenden Proteine von HCV und Plasmodium benötigt werden, um Zielzellen erfolgreich zu infizieren. Unser Ziel ist es, die molekularen Funktionen dieser neuen Wirtsfaktoren umfänglich zu untersuchen. Mittels Mutationsanalysen klären wir auf, wie diese Proteine den Eintritt des Erregers ermöglichen und ob humane Varianten eine unterschiedliche Suszeptibilität zur Folge haben. Gleichzeitig analysieren wir die Spezifität der gefunden Faktoren. Dazu führen wir Infektionsstudien mit anderen umhüllten Viren, mit verschiedenen HCV Genotypen sowie mit humanen als auch Nager Plasmodium Spezies in CRISPR/Cas9 Knockout-Zelllinien durch. Zuletzt untersuchen wir, ob die Wirtsfaktoren zu dem engen Tropismus von HCV und Plasmodium falciparum beitragen. Diese Arbeit wird molekulare Mechanismen der Infektion zweier wichtiger humaner Erreger und dringend benötigte Arzneimitteltargets im Kampf gegen Malaria aufdecken.
Kooperationspartner: Olivier Silvie (INSERM, Paris, Frankreich), Felix Meissner (Max-Planck-Institut für Biochemie, Martinsried), Lars Kaderali (Universität Greifswald)
In unserer bisherigen Forschung gelang es uns, 33 CD81 PPI in humanen Hepatomzellen zu identifizieren, wobei mindestens zehn von diesen CD81 Interaktionspartnern von HCV und Plasmodium benötigt werden, um Zielzellen erfolgreich zu infizieren. Zu diesen Proteinen gehören der Epidermale Wachstumsfaktor Rezeptor (EGFR), eine Rezeptor-Tyrosinkinase, welche in Zusammenhang mit HCV Eintritt beschrieben ist, eine Ubiquitin-Ligase und eine Endopeptidase. Unser Ziel ist es, die molekularen Funktionen dieser Wirtsfaktoren umfänglich zu untersuchen. Mit verschiedenen Domänenmutationen in den Wirtsfaktoren versuchen wir aufzuklären, wie diese Proteine den Eintritt des Erregers ermöglichen. Gleichzeitig analysieren wir die Spezifität der gefunden Interaktionen. Dazu führen wir Infektionsstudien mit anderen umhüllten Viren, mit verschiedenen HCV Genotypen sowie mit humanen als auch Nager Plasmodium Spezies in CRISPR/Cas9 Knockout-Zelllinien für den jeweiligen Eintrittsfaktor durch. Zuletzt untersuchen wir, ob die Wirtsfaktoren zu dem engen Wirts-und Gewebetropismus von HCV und Plasmodium falciparum Sporozoiten beitragen. Diese Arbeit wird Gemeinsamkeiten und Unterschiede während des Eintrittes in Hepatozyten von zwei wichtigen humanen Erregern aufdecken und stellt eine erfolgsversprechende Strategie dar, um dringend benötigte Arzneimitteltargets im Kampf gegen Malaria aufzudecken.
Kooperationspartner: Olivier Silvie (INSERM, Paris, Frankreich), Felix Meissner (Max-Planck-Institut für Biochemie, Martinsried), Lars Kaderali (Universität Greifswald)
Publikationen
Identifizierung von Eintrittsfaktoren umhüllter Viren
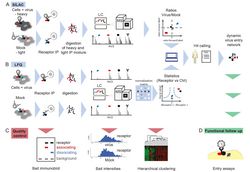
Massenspektrometrie-basierte Interaktionsproteomik hat in den vergangenen Jahren stark an Sensitivität gewonnen und kann mittlerweile quantitative Daten liefern. Mittels neuester Proteomicstechniken identifizieren und untersuchen wir Wirtsfaktoren, die von umhüllten Viren, wie Alphaviren, gebunden werden. Hierbei kombinieren wir speziell entwickelte Anreicherungsmethoden für Proteinkomplexe mit massenspektrometrischen Analysen. Dies erlaubt es uns einerseits, das Interaktom bekannter Eintrittsfaktoren wie des Tetraspanin-9 und TIM-1 mittel markierungsfreier Analyse zu bestimmen („label free quantification“, LFQ). Andererseits nutzen wir stabile Isotopenmarkierung von Aminosäuren in Zellkultur sowie gerichtete Crosslinking Methoden, um solche Proteine zu identifizieren, die mit viralen Hüllporteinen und Rezeptoren beim Zelleintritt oder bei der Replikation interagieren („stable isotope labeling with amino acids in cell culture“, SILAC). Mittels CRISPR/Cas9 Editing, RNA Interferenz und Blockierungsstrategien untersuchen wir in Folgeexperimenten die identifizierten Eintrittsfaktoren.
Unser Hauptaugenmerk liegt derzeit auf den humanpathogenen und Moskito übertragbaren Alphaviren, darunter das Chikungunyavirus. Identifizierte Eintrittsfaktoren und Replikationsfaktoren testen wir anschließend auf ihre Spezifität für verwandte Viren und ihre Expression in verschiedenen humanen Geweben. Zuletzt untersuchen wir, ob verwandte Proteine in Moskitos und Primaten, d.h. im Überträgerwirt und im Reservoirwirt, ebenfalls als Eintrittsfaktoren für Chikungunyavirus fungieren. Diese Arbeit wird beleuchten, wie Alphaviren Wirtszellen infizieren und kann damit zur Entwicklung antiviraler Strategien beitragen.
Unser Hauptaugenmerk liegt derzeit auf humanpathogenen und Moskito übertragbaren Alphaviren sowie auf Norovirus. Identifizierte Eintrittsfaktoren und Rezeptoren testen wir anschließend auf ihre Spezifität für verwandte Viren und ihre Expression in verschiedenen humanen Geweben. Zuletzt untersuchen wir, ob verwandte Proteine in Moskitos und Primaten, d.h. im Überträgerwirt und im Reservoirwirt, ebenfalls als Eintrittsfaktoren für Chikungunyavirus fungieren. In Kooperation mit Niklas Arnberg (Umea University) und Lennart Svensson (Linköping University) führen wir funktionelle Experimente zum Norovirus Eintritt durch. Diese Arbeiten werden beleuchten, wie Alphaviren und Norovirus Wirtszellen penetrieren und können damit zur Entwicklung antiviraler Strategien beitragen.
Kooperationspartner: Margaret Kielian (Albert Einstein College, New York, NY, USA), Christine Goffinet (TWINCORE, Hannover), Pierre-Yves Lozach (Universitätsklinikum Heidelberg), Charles M. Rice (Rockefeller University, New York, NY, USA, Niklas Arnberg (Umea University, Sweden), Lennart Svensson (Linköping University, Sweden)
Publikationen
HCV – Arenavirus Koinfektion und Modulation von angeborenen Immunmechanismen
HCV ist ein kleines, umhülltes RNA Virus und der Erreger der Hepatitis C. Das Virus verursacht chronische Infektionen in 71 Millionen Menschen weltweit und kann schwere Leberschäden auslösen, darunter Zirrhose, Fibrose und Leberkrebs. In vielen Ländern wird eine HCV Infektion nicht diagnostiziert und es ist davon auszugehen, dass in Afrika eine hohe Prävalenz zu finden ist. In diesen Regionen kommt es auch zu Ausbrüchen hämorrhagischer Fieberviren, wie des Lassavirus und Bunyaviren wie das Rifttal Fiebervirus. Da eine chronische Hepatits C Infektion den Immunstatus der Leber verändert, untersuchen wir in Zellkulturmodellen, wie sie sich auf eine sekundäre Infektion mit Arena- und Bunyaviren auswirkt. Insbesondere betrachten wir hierbei die Viruslast, zelluläre Immunerkennungsmechnismen und die Wirksamkeit von antiviralen Medikamenten. Diese Untersuchungen können helfen, Risiken einer zugrundeliegenden chronischen Hepatitis C während Arena- und Bunyavirus Ausbrüchen abzuschätzen.
Diese Arbeiten werden durch die Deutsche Leberstiftung gefördert (S1 63/10135/2017)
Kooperationspartner: Stefan Kunz (CHUV, Lausanne, Schweiz), Friedemann Weber (Universität Gießen), Magnus Evander (Umea University, Sweden), Clas Ahlm (Umea University, Sweden).
Charakterisierung von CD81 Rezeptor-Interaktionen bei der Hepatozyten Invasion von Hepatitis C Virus und Plasmodium
Bruening J, Banse P, Kahl S, Vondran FW, Kaderali L, Marinach C, Silvie O, Pietschmann T, Meissner F*, Gerold G* (2018) Hepatitis C virus enters liver cells using the CD81 receptor complex proteins calpain-5 and CBLB. Manuscript accepted for publication at PLOS Pathogens. *these authors contributed equally
Lasswitz L, Chandra N, Arnberg N*, Gerold G* (2018) Glycomics and proteomics approaches to investigate early adenovirus - host cell interactions. J Mol Biol. doi: 10.1016/j.jmb.2018.04.039. *these authors contributed equally
Banse P, Bruening J, Lasswitz L, Kahl S, Khan AG, Marcotrigiano J, Pietschmann T, Gerold G (2018) CD81 receptor regions outside the large extracellular loop determine hepatitis C virus susceptibility. Viruses doi: 10.3390/v10040207.
Gerold G, Bruening J, Weigel B, Pietschmann T (2017) Protein interactions during the flavivirus and hepacivirus life cycle. Mol Cell Proteomics. pii: mcp.R116.065649.
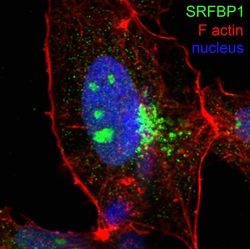
Gerold G, Meissner F, Bruening J, Welsch K, Perin PM, Thomas F. Baumert, Vondran FW, Kaderali L, Marcotrigiano J, Khan AG, Mann M, Rice CM, Pietschmann T (2015) Quantitative Proteomics Identifies Serum Response Factor Binding Protein 1 as a Host Factor for Hepatitis C Virus Entry. Cell Reports. 4;12(5):864-78.
Funding: DFG (GE 2145/3-1), DFG (GE 2145/3-2), DFG (SFB900-C7), DZIF (TI 07.003), Deutsche Leberstiftung (S163/10073/2011), HFSPO (LT000048/2009-L).
Identifizierung von Eintrittsfaktoren Moskito-übertragbarer und gastrointestinaler Viren
Fedeli C, Torriani G, Galan-Navarro C, Moraz ML, Moreno H, Gerold G, Kunz S (2018) Axl Can Serve as Entry Factor for Lassa Virus Depending on the Functional Glycosylation of Dystroglycan. J Virol. doi: 10.1128/JVI.01613-17.
von Schaewen M, Dorner M, Hueging K, Foquet L, Gerges S, Hrebikova G, Heller B, Bitzegeio J, Doerrbecker J, Horwitz J, Gerold G, Suerbaum S, Rice CM, Meuleman P, and Pietschmann T, Ploss A (2016) Expanding the host range of hepatitis C virus through viral adaptation. MBio. 8;7(6).
Scull MA, Shi C, de Jong YP, Gerold G, Ries M, von Schaewen M, Donovan BM, Labitt RN, Horwitz JA, Gaska JM, Hrebikova G, Xiao JW, Flatley B, Fung C, Chiriboga L, Walker CM, Evans DT, Rice CM, Ploss A. (2015) Hepatitis C virus infects rhesus macaque hepatocytes and simianized mice. Hepatology. 62(1):57-67.
Gerold G, Bruening J, Pietschmann T. (2015) Decoding protein networks during virus entry by quantitative proteomics. Virus Research. 218:25-39.
Kapoor A, Simmonds P, Gerold G, Qaisar N, Jain K, Henriquez JA, Firth C, Hirschberg DL, Rice CM, Shields S, Lipkin WI. (2011) Characterization of a canine homolog of hepatitis C virus. PNAS. 108(28):11608-13.
Funding: DFG (GE 2145/3-2), German Liver Foundation (S163/10135/2017), DAAD, ZIB, Friends of the MHH.