Projekte Translationale Immunologie

Gewebe-spezifische Entzündung bei chronisch-rheumatischen Erkrankungen
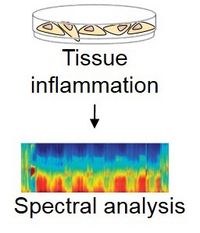
Patienten mit chronisch rheumatischen Erkrankungen leiden unter häufigeren und schwereren Verläufen von Infektionen. Insbesondere eine hohe Entzündungsaktivität erhöht das Risiko für zusätzliche Infektionen. Zudem können sich Entzündungsreaktionen in unterschiedlichen Geweben erheblich unterscheiden. Ziel dieses Projektes ist es die Entzündungsreaktionen rheumatischer Erkrankungen in unterschiedlichen Geweben besser zu verstehen, um anschließend die spezifische Entzündung besser behandeln zu können. So kann sowohl die Symptomatik der Grunderkrankung, als auch das Risiko resultierender Infektionen reduziert werden.
Ein besonderer Schwerpunkt liegt hier in der Erforschung der Pathophysiologie der systemischen Sklerose. Anders als andere Erkrankungen aus der Gruppe der Kollagenosen ist die Krankheitsentstehung bei der systemischen Sklerose unklar. Betroffene Patienten leiden unter schweren Entzündungen der Haut und Blutgefäße, der Lunge und des Herzens. In enger Kooperation mit der Medizinischen Hochschule Hannover werden Immunzellen aus entzündeten Geweben betroffener Patienten isoliert und detailliert analysiert. So sollen neue Angriffspunkte für Therapien dieser Erkrankung identifiziert werden.
Förderung
Hannover Biomedical Research School (HBRS) and the Centre for Infection Biology (ZIB); DFG-funded "International research training group" (IRTG) 1273; Deutsche Forschungsgemeinschaft (DFG) Klinische Forschergruppe (KFO 250)
Indirekte Wirkungen immunmodulatorischer Medikamente
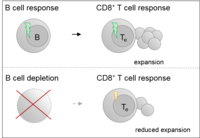
Zur Behandlung chronisch rheumatischer Erkrankungen ist eine Vielzahl immunmodulatorischer Medikamente zugelassen. Die Wirkungsweise dieser Medikamente beruht in der Blockade einzelner Botenstoffe, wie Zytokine, der direkten Bindung und Beeinflussung von Rezeptoren verschiedener Immunzellen, oder sogar der ganzen Depletion eines Immunzell-Subtyps. Da Immunzellen eng kommunizieren und kooperieren kann die Beeinflussung eines Immunzell-Subtyps auch indirekte Effekte auf andere Immunzellen haben. Insbesondere während Infektionen und bei Impfungen ist es wichtig, die Wirkung dieser Medikamente auf das Immunsystem zu kennen, um optimale Immunantworten erzeugen zu können. Ziel dieses Projektes ist es deshalb den Einfluss Immunmodulatorischer Medikamente auf Impfantworten zu erforschen und passende Medikamente für individuelle Patientengruppen zu identifizieren, die einen optimalen Impferfolg erlauben.
Förderung
DFG, German Research Foundation grant SFB900; Germany's Excellence Strategy – EXC 2155 “RESIST”; Deutsche Forschungsgemeinschaft (DFG) Klinische Forschergruppe (KFO 250)
Zielgerichtete Therapie von Immunzellen
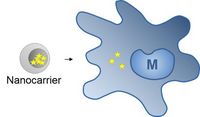
Der systemische Einsatz immunmodulatorischer Medikamente kann auch systemische unerwünschte Arzneimittelwirkungen nach sich ziehen. Liposomale oder synthetische Nanocarrier können Medikamente direkt in Zielzellen einschleusen. Dafür ist ein spezifischer zielgerichteter Transport in die entsprechende Zielzelle notwendig. In diesem Projekt soll der Einsatz verschiedener Nanocarrier zum Einschleusen von Wirkstoffen in myeloide Immunzellen getestet werden. Ein direktes Einschleusen von Medikamenten in Zielzellen kann systemische Nebenwirkungen reduzieren und gleichzeitig lokale Wirkspiegel deutlich erhöhen.
Förderung:
German Federal Ministry of Economics and Technology (BMWi), via the Consortium of Industrial Research Associations (AiF), ZIM Program, Grant KF2531702AJ3; DFG, German Research Foundation grant SFB900; Germany's Excellence Strategy – EXC 2155 “RESIST”
Hirche C, Frenz T, Haas S, Döring M, Borst K, Tegtmeyer P, Brizic I, Jordan S, Keyser K, Chhatbar C, Pronk E, Lin S, Messerle M, Jonjic S, Falk CS, Trumpp S, Essers M, Kalinke U (2017) Systemic virus infections differentially modulate cell cycle state and functionality of long-term hematopoietic stem cells in vivo. Cell Rep 19(11): 2345-2356.
Borst K, Frenz T, Spanier J, Tegtmeyer PK, Chhatbar C, Skerra J, Ghita L, Namineni S, Lienenklaus S, Koster M, Heikenwaelder M, Sutter G, Kalinke U (2018) Type I interferon receptor signaling delays Kupffer cell replenishment during acute fulminant viral hepatitis. J Hepatol 68(4): 682-690.
Frenz T, Grabski E, Buschjager D, Vaas LA, Burgdorf N, Schmidt RE, Witte T, Kalinke U (2016) CD4+ T cells in patients with chronic inflammatory rheumatic disorders show distinct levels of exhaustion. J Allergy Clin Immunol 138(2): 586-589 e10.
Graalmann T, Borst K, Manchanda H, Vaas L, Bruhn M, Graalmann L, Koster M, Verboom M, Hallensleben M, Guzman CA, Sutter G, Schmidt RE, Witte T, Kalinke U (2021) B cell depletion impairs vaccination-induced CD8(+) T cell responses in a type I interferon-dependent manner. Ann Rheum Dis (in press).
Frenz T, Grabski E, Buschjager D, Vaas LA, Burgdorf N, Schmidt RE, Witte T, Kalinke U (2016) CD4+ T cells in patients with chronic inflammatory rheumatic disorders show distinct levels of exhaustion. J Allergy Clin Immunol 138(2): 586-589 e10.
Duran V, Grabski E, Hozsa C, Becker J, Yasar H, Monteiro JT, Costa B, Koller N, Lueder Y, Wiegmann B, Brandes G, Kaever V, Lehr CM, Lepenies B, Tampe R, Forster R, Bosnjak B, Furch M, Graalmann T, Kalinke U (2021) Fucosylated lipid nanocarriers loaded with antibiotics efficiently inhibit mycobacterial propagation in human myeloid cells. J Control Release 334: 201-212.
Frenz T, Grabski E, Duran V, Hozsa C, Stepczynska A, Furch M, Gieseler RK, Kalinke U (2015) Antigen presenting cell-selective drug delivery by glycan-decorated nanocarriers. Eur J Pharm Biopharm 95(Pt A): 13-17.